Системний пристрій StrongStep для швидкого тесту антигену SARS-COV-2
Призначене використання
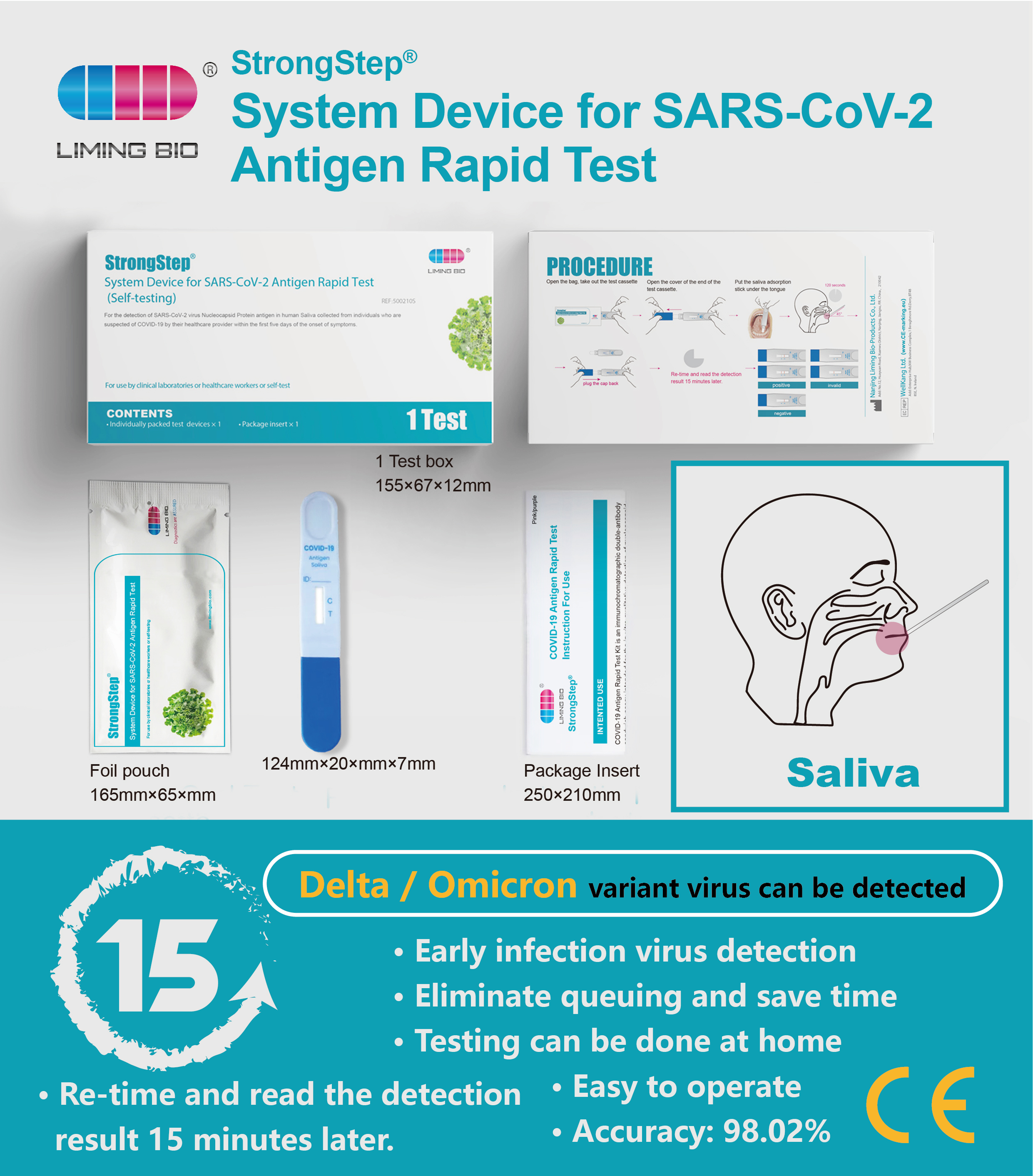
Системний пристрій StrongStep® для швидкого тестування антигену SARS-2 використовує технологію імунохроматографії для виявлення нуклеокапсидного антигену SARS-COV-2 в слині людини. Цей тест є єдиним використанням і призначений для SEI - тестування. Рекомендується використовувати цей тест протягом 7 днів після початку симптомів, він підтримується клінічною оцінкою ефективності.
Вступ
Роман коронавіруси належать до роду 0. Covid-19-гостре респіраторне інфекційне захворювання. Люди, як правило, сприйнятливі. В даний час пацієнти, заражені новим коронавірусом, є основним джерелом інфекції, заснованої на поточному епідеміологічному дослідженні, інкубаційний період становить від 1 до 14 днів, переважно від 3 до 7 днів. Основні прояви включають лихоманку, втому та сухий кашель. Носова затори, нежить, біль у горлі, міалгія та діарея виявляються в кількох випадках.
Принцип
Системний пристрій StrongStep® для тесту на антиген SARS-COV-2 використовує імунохроматографічний тест, цей комплект збирає зразки слини з адсорбційної палички слини в передній частині тестової картки, а зразки слини рухаються вперед під капілярною дією. Якщо зразок містить антиген протеїну SARS-COV-2 N. Він ідентифікований і пов'язаний антитілами, позначеними на поверхні латексу, утворюючи імунний комплекс. Коли утворений імунний комплекс мігрує до лінії виявлення мембран азотної кислоти, для ідентифікації упакованих антитіл та утворення лінії виявлення фуксії (Т-лінійки), що демонструє антиген-позитивне антиген-2; Якщо Т-лінія не показує кольору, це негативний результат. Інша лінія на мембрані азотної кислоти упакована антитілами стрептавідин як лінії контролю якості (лінія C), щоб вказати на ефективний процес тестування.
ЗАПОБІЖНІ ЗАХОДИ
• Цей комплект призначений лише для діагностичного використання in vitro.
• Цей комплект може вводити медичний або немедичний персонал, дотримуючись інструкцій з експлуатації.
• Уважно прочитайте інструкції перед проведенням тесту.
• Цей продукт не містить жодних матеріалів людини.
• Не використовуйте вміст набору після терміну придатності.
• Обробляйте всі зразки як потенційно інфекційні.
• Не реагенту на піпетку і не куріння та не їжі під час проведення аналізів.
• Носіть рукавички протягом усієї процедури.
Зберігання та стабільність
Герметичні сумки в тестовому наборі можуть зберігатися між 2-30 ° С протягом тривалості терміну придатності, як зазначено на сумці.
Колекція та зберігання зразків
Найкращий зразок слини повинен бути зібраний вранці після просто прокидання. Не їжте і не пийте нічого за 30 хвилин до збору зразка слини. Зробіть це перед тим, як випити каву, снідати або чистити зуби - або чекати, поки ви нічого не спожили за попередні 30 хвилин.
Процедура
Перед використанням принесіть випробування до кімнатної температури (15-30 ° C).
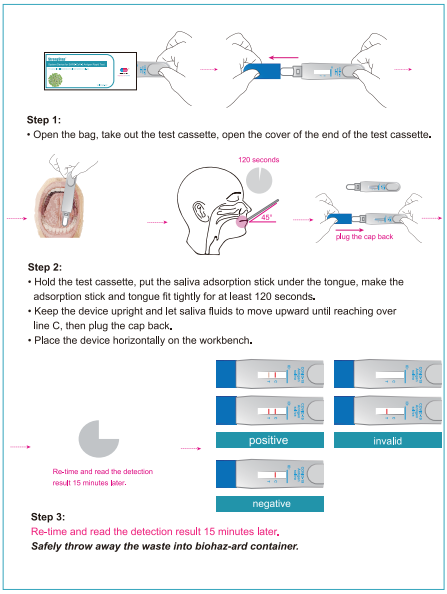
Крок 1:
Відкрийте сумку, вийміть тестовий пристрій, відкрийте кришку кінця тестового пристрою.
Крок 2:
• Тримайте ламку касету, покладіть під язик адсорбційну паличку слини, зробіть адсорбційну паличку і язик щільно підходять не менше 120 секунд.
• Тримайте пристрій вертикально і дозволяйте слиною рідинам рухатися вгору до досягнення лінії C, а потім підключіть кришку назад.
• Розмістіть пристрій горизонтально на робочому столі.
Крок 3:
Переробляйте час і прочитайте виявлення Resuh через 15 хвилин.
Безпечно викиньте відходи в контейнер Biohaz-Ard.
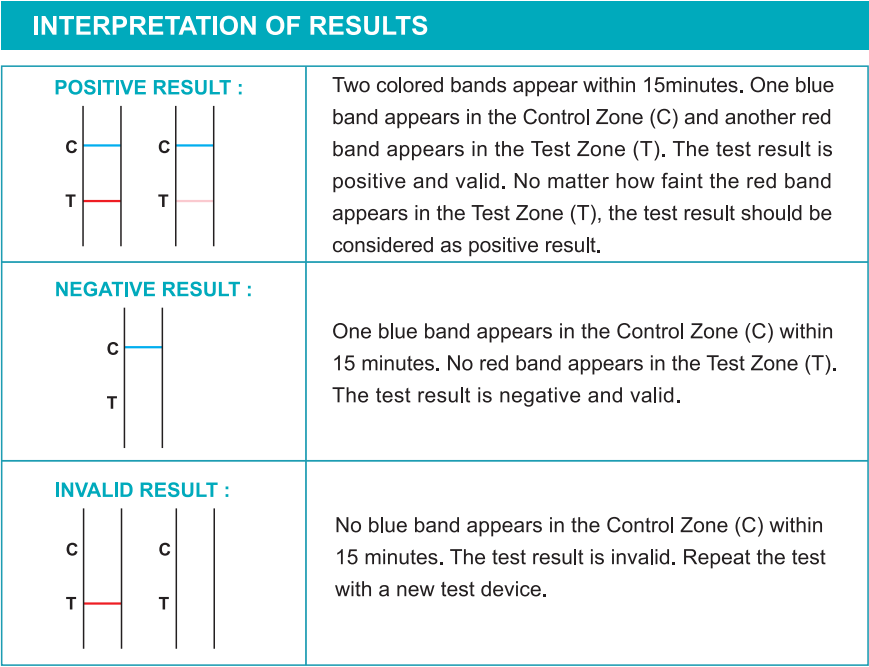
Контроль якості
Внутрішній процедурний контроль включається в тест. Синя смуга, що з’являється в контрольній області (С), розглядається як внутрішній процедурний контроль. Він підтверджує достатній об'єм зразка та правильну процедурну техніку.
Обмеження тесту
1. Комплект призначений для використання для якісного виявлення антигенів SARS-COV-2 зі слини.
2. Цей тест виявляє як життєздатні (живі), так і нежиттєздатні SARS-COV-2. Виконання тесту залежить від кількості вірусу (антигену) у зразку і може не співвідноситись з результатами вірусної культури, виконаними на одному зразку.
3. Негативний результат тесту може виникнути, якщо рівень антигену в зразку нижче межі виявлення тесту або якщо зразок збирали або транспортували неправильно.
4. Недотримання процедури тестування може негативно вплинути на ефективність тесту та/або недійсним результат тесту.
5. Комплект призначений лише для передбачуваного скринінгу. Негативні результати не виключають інфекції SARS-COV-2, і людина не інфекційна. Якщо симптоми присутні, зверніться до негайного подальшого тестування.
6. Результати тестів повинні бути співвіднесені з клінічною історією, епідеміологічними даними та іншими даними, доступними клініці, оцінюючи пацієнта.
7. Позитивні результати тестування не виключають спільних інфекцій з іншими збудниками і не можуть обов'язково визначати, чи людина інфекційна.
8. Негативні результати тестування не призначені для правління в інших вірусних або бактеріальних інфекціях.
9. Негативні результати пацієнтів із симптомом слід розглядати як передбачувані та підтверджені місцевим молекулярним аналізом FDA, якщо це необхідно, для клінічного управління, включаючи контроль інфекції.
201 Користувачі повинні перевірити зразки якомога швидше після колекції зразків.
11. Чутливість до аналізу RT-PCR при діагностиці Covid-19 становить лише 50% -80% через погану якість якості вибірки або часовий момент захворювання на фазі відновлення тощо. нижчий через його методологію.
12. Позитивні та негативні прогнозні значення сильно залежать від швидкості поширеності.
Позитивні результати тестування мають більше шансів представляти помилкові позитивні результати в періоди активності мало / відсутність SARS-COV-2, коли поширеність захворювання низька. Результати негативних тестів уфалзових є більш імовірними, коли поширеність захворювання, спричинене SARS-COV-2, є високою.
13. Моноклональні антитіла можуть не виявити або виявити з меншою чутливістю, віруси грипу-2-2, які зазнали незначних змін амінокислот в області цільової епітопів.
14. Продуктивність цього тесту не була оцінена для використання пацієнтам без ознак та симптомів дихальної інфекції та ефективності може відрізнятися у безсимптомних осіб.
15. Кількість антигену в зразку може зменшуватися зі збільшенням тривалості хвороби.
Зразки, зібрані після 7-го дня хвороби, швидше є негативними порівняно з аналізом RT-PCR.
Відомо, що чутливість тесту після семи днів виникнення симптомів зменшилася порівняно з аналізом RT-PCR.
16. Не рекомендується використовувати зразок вірусних транспортних засобів (VTM) у цьому тесті, якщо клієнти наполягають на тому, щоб використовувати цей тип зразка, клієнти повинні підтвердити себе.
17. Часте тестування необхідно для підвищення чутливості діагностики Коженда-19.
18. Без випадання чутливості у порівнянні з диким типом щодо наступних варіантів -B.1.1.7; B.1.351; B.1.2; B.1.1.28; B.1.617; B.1.1.529.
19. Позитивні результати свідчать про те, що вірусні антигени були виявлені у взятому зразку, будь ласка, будь ласка, самостійно та повідомте свого сімейного лікаря та/або місцевого департаменту охорони здоров'я відповідно до державних вимог.
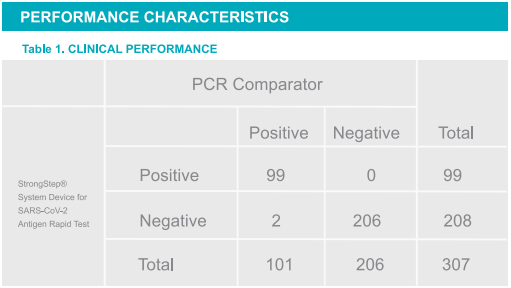
Позитивний відсоток домовленості: (PPA) = 98,02%(93,03%~ 99,76%)*
Негативний відсоток домовленості: (NPA) = 100%(98,23%~ 100%)*
Загальний рівень збігу = 98,76%
*95%довірчий інтервал
Аналітична ефективність
а) межа виявлення (LOD):
Межу виявлення (LOD) тесту визначали за допомогою обмежувальних розведення інактивованих SARS-COV-2. Це підготовка коронавірусу-2, пов'язаного з ГРВО (SARS-COV-2), ізолюючи в Китаї CDC, який був інактивований β-пропіолактоном. Матеріал подавали заморожені в концентрації TCID505,00 X105/мл.
Для визначення SARS-COV-2 для відображення аналізу при використанні прямої слини. У цьому дослідженні приблизно 50 мкл розведення вірусу піднімали негативним зразком слини.
LOD визначали в три етапи:
1. Скринінг LOD
10-кратне розведення інактивованого вірусу проводили в негативній слині та обробляли для кожного дослідження, як описано вище. Ці розведення тестували в трьох примірниках. Концентрація, що демонструє 3 з 3 позитивів, була обрана для пошуку діапазону LOD.
2. Значення діапазону LOD
П'ять (5) подвоєння розведення було зроблено з TCID505,00 X102/мл концентрація в негативній слині, обробленій для дослідження, як описано вище. Ці розведення тестували в трьох примірниках. Для підтвердження LOD було обрано концентрацію, що демонструє 3 з 3 позитивів.
3. Підтвердження LOD
Концентрація tcid502,50 x102/Мл розведення тестували на загальну кількість двадцяти (20) результатів. Принаймні дев'ятнадцять (19) двадцяти (20) результатів були позитивними.
Висновок:
Виходячи з цього тестування, концентрація була підтверджена як:
LOD: TCID502,50 x102/мл
б) Перехресна реакція:
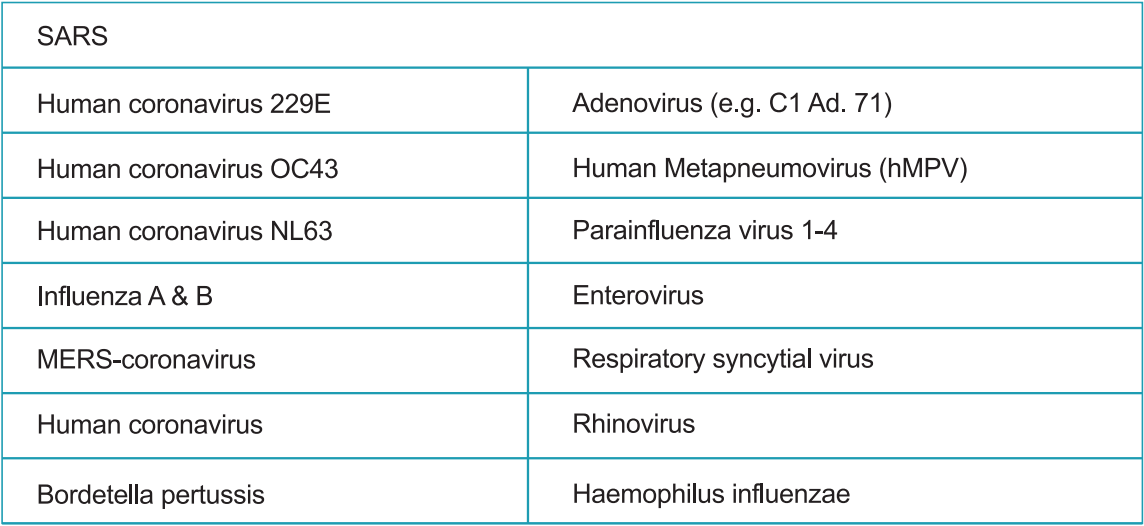
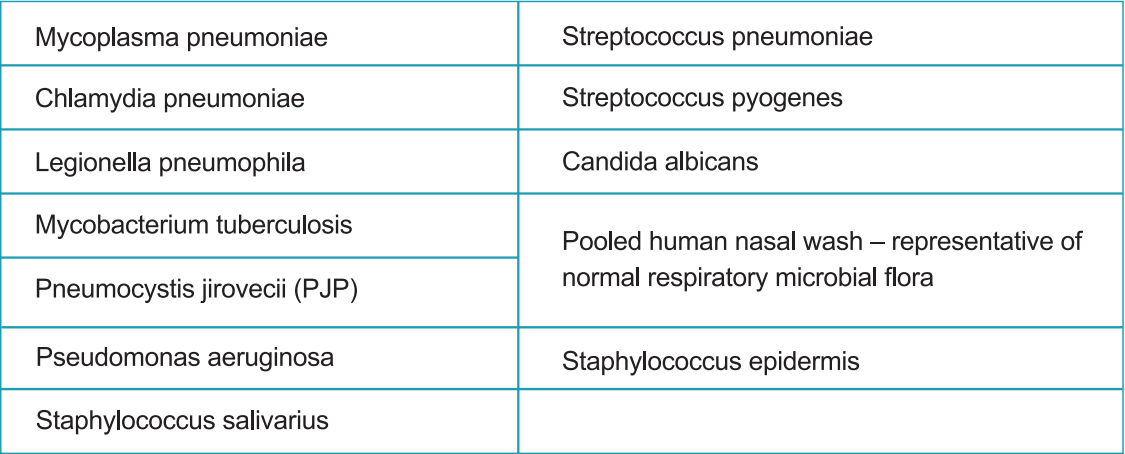
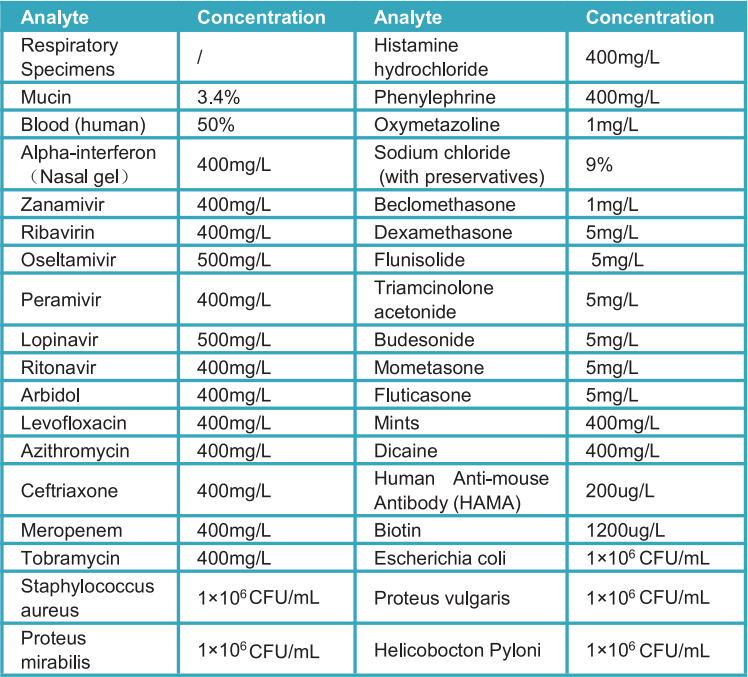
Перехресна реактивність системного пристрою StrongStep® SARS-COV-2 Швидкий тест антигену оцінювали шляхом тестування різних мікроорганізмів (10⁶ CFU/мл), вірусів (10⁵ PFU/мл) та негативних матрикатів, які потенційно можуть перехресно перехитуватися з Strongstep® Системний пристрій SARS-COV-2 швидкий тест.
Кожен організм та вірус тестували в трьох примірниках. На основі даних, отриманих за допомогою цього дослідження, системний пристрій StrongStep® для швидкого тесту антигену SARS-COV-2 не перехресно реагує з тестуваними організмами або вірусами.
в) втручання речовини:
Потенційні перешкоджаючі речовини швидкого тесту антигену StrongStep® SARS-COV-2 оцінювали шляхом тестування різних речовин із концентрацією нижче, що може потенційно заважати швидкому тесту антигену VARS-COV-2. Кожну речовину тестували в трьох примірниках. На основі даних, отриманих за допомогою цього дослідження, швидкий тест антигену StrongStep® SARS-COV-2 не заважає випробуваним речовинам.
г) ефект гачка
Найвища концентрація тепло-інактивованих запасів SARS-COV-2 (TCID505,00 х 105/мл) тестували. Ефект гака не виявлено.




1人份抗原卡实物图唾液版1_00_副本-300x216.png)